ЭФФЕКТИВНОСТЬ И БЕЗОПАСНОСТЬ ДЖЕНЕРИКОВ СОФОСБУВИРА И ЛЕДИПАСВИРА(КРАТКИЙ ОБЗОР СТАТЬИ)
ЭФФЕКТИВНОСТЬ И БЕЗОПАСНОСТЬ ДЖЕНЕРИКОВ СОФОСБУВИРА И ЛЕДИПАСВИРА(КРАТКИЙ ОБЗОР СТАТЬИ)
Статья в русской версии журнала Journal of Hepatology: «Воспроизведенный препарат Сфосбувира-Ледипасвира для пациентов с хроническим гепатитом C: обсервационное исследование в реальной клинической практике.
Актуальность и цели. В развивающихся странах немногие пациенты с гепатитом C могут позволить себе лечение оригинальными противовирусными препаратами прямого действия, в то же время существуют сомнения в биоэквивалентности воспроизведенных препаратов.
Настоящее исследование было посвящено оценке безопасности и эффективности приема в течение 8 или 12 нед. воспроизведенного препарата Софосбувира-Ледипасвира в сочетании с Рибавирином или без него у пациентов из Китая с гепатитом C генотипа 1b.
Методы. В этом открытом обсервационном исследовании участвовало 63 пациента с циррозом (группа 1) и 65 пациентов без цирроза печени (группа 2), которые получали воспроизведенный препарат Софосбувира-Ледипасвира + 1000–1200 мг Рибавирина в сутки в течение 12 и 8 нед. соответственно, а также 64 пациента без цирроза (группа 3), получавшие оригинальный Софосбувира-Ледипасвир в течение 8 нед.
Первичным показателем эффективности считалась неопределяемая РНК HCV через 12 нед. после окончания лечения (УВО12).
Также собирались данные по безопасности и фармакокинетике.
Результаты. Лечение завершило 187 пациентов; при последнем анализе на 5-й неделе лечения РНК HCV была ниже определияемого уровня у 3 пациентов с циррозом. Анализ у всех пациентов, начавших лечение, показал частоту УВО12 96,8 (61 из 63), 96,9 (63 из 65) и 96,9 % (62 из 64) в группах 1, 2 и 3 соответственно.
У 1 пациента в группе 3 отмечен рецидив на 4-й неделе после окончания лечения.
Схемы терапии в целом хорошо переносились. Наиболее частыми нежелательными явлениями были слабость (17,8 %), диарея (10,9 %) и головная боль (9,9 %).
4 пациента прервали лечение из-за диареи и рвоты. 1 пациентка из группы 2 прервала лечение на 29-й день из-за невозможности приобрести препарат; к счастью, она достигла УВО12.
Таким образом настоящее исследование показало, что 8 или 12 нед. приема воспроизведенного препарата Софосбувира-Ледипасвира в сочетании с Рибавирином или без него безопасно и эффективно у пациентов с гепатитом C генотипа 1b.
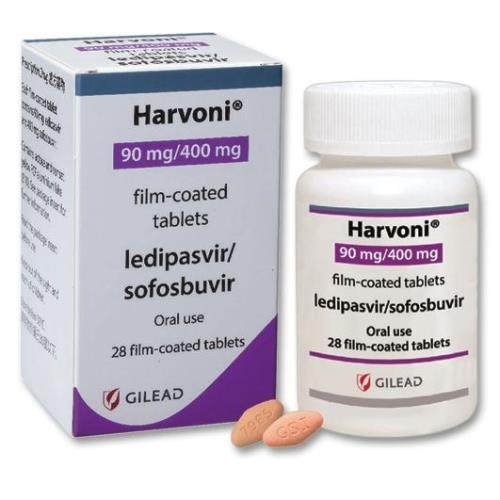
ВЫВОД: Высокая стоимость Харвони® ограничивает доступ к препарату для пациентов многих развивающихся и некоторых развитых стран с небольшим бюджетом на нужды здравоохранения. Компания Gilead одобрила воспроизведенный препарат Софосбувира-Ледипасвира, стоимость которого намного ниже, чем у Харвони®, и который обеспечивает ту же частоту излечения пациентов с хроническим гепатитом C.
СПРАВКА: термин «воспроизведенный препарат» ,то есть «дженерик», «генерированная форма препарата» (англ. generic drug).
На фото ниже представлены: оригинальный препарат Harvoni(GILEAD. USA) и воспроизведенный препарат(дженерик) Hepcinat LP(Natco. India).

Статья в русской версии журнала Journal of Hepatology: «Воспроизведенный препарат Сфосбувира-Ледипасвира для пациентов с хроническим гепатитом C: обсервационное исследование в реальной клинической практике.
Актуальность и цели. В развивающихся странах немногие пациенты с гепатитом C могут позволить себе лечение оригинальными противовирусными препаратами прямого действия, в то же время существуют сомнения в биоэквивалентности воспроизведенных препаратов.
Настоящее исследование было посвящено оценке безопасности и эффективности приема в течение 8 или 12 нед. воспроизведенного препарата Софосбувира-Ледипасвира в сочетании с Рибавирином или без него у пациентов из Китая с гепатитом C генотипа 1b.
Методы. В этом открытом обсервационном исследовании участвовало 63 пациента с циррозом (группа 1) и 65 пациентов без цирроза печени (группа 2), которые получали воспроизведенный препарат Софосбувира-Ледипасвира + 1000–1200 мг Рибавирина в сутки в течение 12 и 8 нед. соответственно, а также 64 пациента без цирроза (группа 3), получавшие оригинальный Софосбувира-Ледипасвир в течение 8 нед.
Первичным показателем эффективности считалась неопределяемая РНК HCV через 12 нед. после окончания лечения (УВО12).
Также собирались данные по безопасности и фармакокинетике.
Результаты. Лечение завершило 187 пациентов; при последнем анализе на 5-й неделе лечения РНК HCV была ниже определияемого уровня у 3 пациентов с циррозом. Анализ у всех пациентов, начавших лечение, показал частоту УВО12 96,8 (61 из 63), 96,9 (63 из 65) и 96,9 % (62 из 64) в группах 1, 2 и 3 соответственно.
У 1 пациента в группе 3 отмечен рецидив на 4-й неделе после окончания лечения.
Схемы терапии в целом хорошо переносились. Наиболее частыми нежелательными явлениями были слабость (17,8 %), диарея (10,9 %) и головная боль (9,9 %).
4 пациента прервали лечение из-за диареи и рвоты. 1 пациентка из группы 2 прервала лечение на 29-й день из-за невозможности приобрести препарат; к счастью, она достигла УВО12.
Таким образом настоящее исследование показало, что 8 или 12 нед. приема воспроизведенного препарата Софосбувира-Ледипасвира в сочетании с Рибавирином или без него безопасно и эффективно у пациентов с гепатитом C генотипа 1b.
ВЫВОД: Высокая стоимость Харвони® ограничивает доступ к препарату для пациентов многих развивающихся и некоторых развитых стран с небольшим бюджетом на нужды здравоохранения. Компания Gilead одобрила воспроизведенный препарат Софосбувира-Ледипасвира, стоимость которого намного ниже, чем у Харвони®, и который обеспечивает ту же частоту излечения пациентов с хроническим гепатитом C.
СПРАВКА: термин «воспроизведенный препарат» ,то есть «дженерик», «генерированная форма препарата» (англ. generic drug).
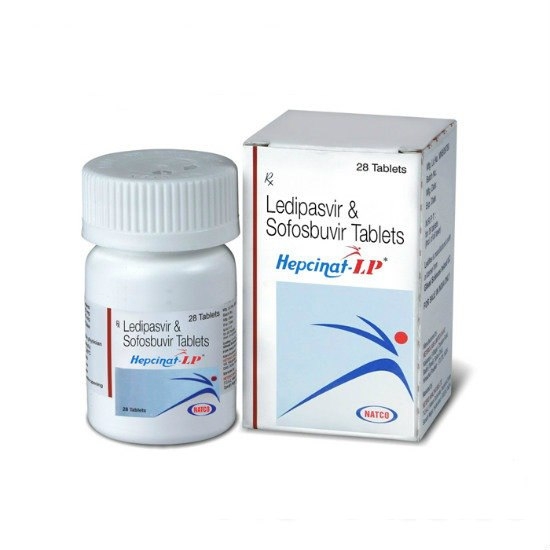
На фото ниже представлены: оригинальный препарат Harvoni(GILEAD. USA) и воспроизведенный препарат(дженерик) Hepcinat LP(Natco. India).

